- Категория
- Новости
В США одобрен противозачаточный пластырь для замены пероральных контрацептивов
- Дата публикации
- Количество просмотров
-
1285
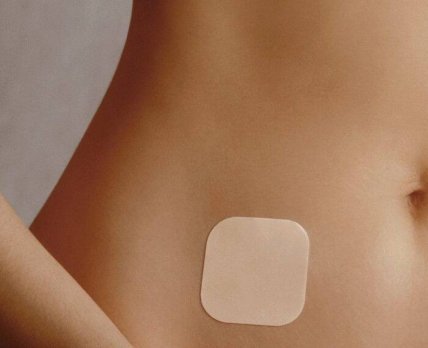
FDA ободрило противозачаточный патч Twirla от компании Agile Therapeutics, он может применяться как альтернатива пероральным контрацептивам. Продажи начнутся уже в конце 2020 года.
Как сообщил в пресс-релизе производитель Agile Therapeutics, FDA утвердило противозачаточный пластырь компании Twirla. Патч Twirla содержит 30 мкг левоноргестрела и 120 мкг этинилэстрадиола и меняется еженедельно. Патч можно крепить на животе, ягодицах или верхней части туловища, но не на груди. Новый трансдермальный контрацептив обеспечивает уровень эстрогена в соответствии с указанными дозами, аналогичный тому, что и у традиционных пероральных противозачаточных средств.
Этот комбинированный гормональный противозачаточный препарат подходит для женщин репродуктивного возраста без ожирения (с ИМТ менее 30 кг / м2). В инструкции Twirla содержится предупреждение о риске сердечнососудистых событий у женщин в возрасте 35 лет и старше, которые курят и имеют ИМТ более 30 кг / м2. Ряд испытаний 3 фазы показали, что профиль безопасности Twirla аналогичен другим утвержденным противозачаточным средствам. Распространенные побочные эффекты, связанные с использованием пластыря, включали назофарингит, инфекцию верхних дыхательных путей, тошноту и головную боль ИМП. Тяжелые нежелательные явления отмечались менее чем у 2% пациентов и включали желчнокаменную болезнь, тромбоз глубоких вен, легочную эмболию и депрессию.
Agile Therapeutics заявила, что планирует отгрузить первые партии продукта оптовикам в четвертом квартале 2020 года. Agile Therapeutics также сообщила, что FDA требует от компании проведения долгосрочного проспективного наблюдательного постмаркетингового исследования для оценки риска венозной тромбоэмболии и артериальной тромбоэмболии.















